Кузнецов М.Р. 1 , Сапелкин С.В. 2 , Болдин Б.В. 3 , Леонтьев С.Г. 1 , Несходимов Л.А. 3
1) Кафедра факультетской хирургии, урологии, Российский национальный исследовательский медицинский университет им. Н.И. Пирогова,
2) Институт хирургии им. А.В. Вишневского Минздрава РФ,
3) Кафедра факультетской хирургии №2, Российский национальный исследовательский медицинский университет им. Н.И. Пирогова, Москва, Россия
Проанализированы результаты обследования и лечения 102 больных с илиофеморальным венозным тромбозом. В процессе лечения при проведении ультразвукового дуплексного сканирования определяли локализацию проксимальной границы тромботических масс, время появления первых признаков реканализации, ее степень на различных уровнях глубокой венозной системы, изменение скорости венозного кровотока в глубоких венах нижних конечностей. Динамику клинических симптомов оценивали по визуально-аналоговой шкале. Клиническое и инструментальное обследование выполнялось через 10 суток, 1, 3, 6 и 12 месяцев от начала лечения. Больные были разделены на 3 группы. В 1 группу вошли 38 больных, которым проводилась терапия низкомолекулярным гепарином (эноксапарин) с последующим переходом на непрямые антикоагулянты (варфарин) в сочетании с венотониками (оригинальный высокоочищенный диосмин 600 мг 1 раз в сутки). Во 2 группу были включены 33 пациента, получавшие Ривароксабан (Ксарелто) по 15 мг два раза в сутки в течение 3 недель, далее по 20 мг один раз в сутки. Больные 3 группы (31 пациент) также получали Ривароксабан (Ксарелто) по описанной выше стандартной схеме, но в комбинации с венотониками (оригинальный высокоочищенный диосмин 600 мг 1 раз в сутки).
Исследование показало, что назначение больным с первого дня заболевания Ривароксабана (Ксарелто) позволило значительно улучшить и ускорить процессы восстановления проходимости глубоких вен нижних конечностей по сравнению с пациентами, получавшими антагонисты витамина К (варфарин). У больных, принимающих ривароксабан (ксарелто), не выявлено ни одного случая остаточных тромботических окклюзий магистральных вен, а реканализация у трех четвертей пациентов была расценена как хорошая и еще одной четверти – как средней степени. В группе варфарина у 13% больных сохранялась окклюзия в подвздошных венах, а хорошая реканализация наблюдалась только у половины больных. Добавление к антикоагулянтам с первого дня лечения венотоников (оригинального высокоочищенного диосмина) продемонстрировало безопасность этой схемы лечения (ни у одного больного не было выявлено клинически значимых геморрагических осложнений) и ее большую эффективность по сравнению с монотерапией Ривароксабаном (Ксарелто). Комбинация диосмина с Ривароксабаном (Ксарелто) была эффективней, чем сочетание Диосмина и Варфарина.
КЛЮЧЕВЫЕ СЛОВА: острый венозный тромбоз, посттромботическая болезнь, хроническая венозная недостаточность, антикоагулянты, венотоники, ривароксабан (ксарелто), варфарин, диосмин.
Посттромбофлебитическая болезнь (ПТФБ) – одна из наиболее тяжелых форм хронической венозной недостаточности (ХВН), достаточно часто приводящая к развитию трофических расстройств, вплоть до плохо поддающихся лечению трофических язв [1]. Наиболее тяжело протекает ПТФБ после перенесенного илиофеморального флеботромбоза (ИФФТ) [2]. Связано это с недостаточной реканализацией и остаточными окклюзиями на всем протяжении пораженных глубоких вен нижних конечностей, особенно на проксимальном уровне (подвздошные, бедренная вены) [3]. Как правило, процессы реканализации наиболее активно происходят в течение первых 6-12 месяцев после перенесенного острого венозного тромбоза, после чего динамика морфологических изменений в глубоких венах уже не становится столь значимой [4]. Как правило, при сформированной ПТФБ наиболее часто проводят консервативную терапию, несмотря на наличие остаточных участков окклюзий магистральных вен, поскольку хирургические реконструктивные операции имеют плохие результаты как в ближайшем, так и в отдаленном послеоперационном периоде, и могут усугубить явления ХВН [5]. Эндоваскулярные методы лечения пока имеют ограниченное применение в связи с техническими сложностями и отсутствием должного количества наблюдений в отдаленном периоде [6]. В связи с этим возникает потребность адекватного лечения острого венозного тромбоза, позволяющего добиться более полной и быстрой реканализации глубоких вен нижних конечностей [7-9]. При этом высказываются мнения о возможности сочетанного применения антикоагулянтов и венотоников [10].
Цель исследования: оценить эффективность методов консервативного лечения острого венозного тромбоза глубоких вен нижних конечностей c позиций предотвращения или более легкого течения ПТФБ.
Материалы и методы
Проанализированы результаты обследования и лечения 102 больных с ИФФТ. У всех пациентов проксимальный уровень тромба находился выше паховой связки (наружная или общая подвздошные вены). Больные, которым проводилась хирургическая профилактика тромбоэмболии легочной артерии, в настоящее исследование не включались. В процессе лечения при проведении ультразвукового дуплексного сканирования определяли локализацию проксимальной границы тромботических масс, время появления первых признаков реканализации, ее степень на различных уровнях глубокой венозной системы, изменение скорости венозного кровотока в глубоких венах нижних конечностей. Степень реканализации оценивали по методике, разработанной в нашей клинке и внедренной в практическое здравоохранение [11]: 1 – слабая (при компрессии ультразвуковым датчиком сжимается лишь небольшая часть просвета вены, не более 30%); 2 – средняя (при компрессии сжимается около 50% просвета вены); 3 – хорошая (сжимается более 70% просвета вены). Степень выраженности клинических симптомов (тяжесть в ногах, отеки, парестезии) оценивали в динамике по визуально-аналоговой шкале. Наблюдение за всеми больными проводилось в течение одного года. Клиническое и инструментальное обследование выполнялось через 10 суток, 1, 3, 6 и 12 месяцев от начала лечения.
Больные были разделены на 3 группы, сопоставимые по полу, возрасту, сопутствующей патологии и локализации поражения. В 1 группу вошли 38 больных, которым проводилась терапия низкомолекулярным гепарином (эноксапарин) с последующим переходом на непрямые антикоагулянты (варфарин) в сочетании с венотониками (оригинальный высокоочищенный диосмин 600 мг 1 раз в сутки). Во 2 группу были включены 33 пациента, получавшие ривароксабан по 15 мг два раза в сутки в течение 3 недель, далее по 20 мг один раз в сутки. Больные 3 группы (31 пациент) также получали ривароксабан по описанной выше стандартной схеме, но в комбинации с венотониками (оригинальный высокоочищенный диосмин 600 мг 1 раз в сутки). Венотоники, как и антикоагулянты, больные получали с первого дня лечения на протяжении 12 месяцев. Кроме этого, все пациенты носили на протяжении всего срока наблюдения эластический компрессионный трикотаж 2 класса компрессии.
Статистический анализ результатов проводился с использованием непараметрических методов: при сравнении независимых групп применялся U-критерий Манна-Уитни, при сравнении связанных групп (анализ динамики в процессе лечения) – критерий Вилкоксона.
Ни у одного больного во всех трех группах на протяжении всего срока наблюдения (12 месяцев) не было случаев клинически значимых геморрагических осложнений. В то же время у всех пациентов первые признаки реканализации были отмечены на 10 сутки в венах голени, а у ряда больных – и в подколенной вене; при этом статистически значимых различий между группами выявлено не было. В дальнейшем через 1 месяц после начала лечения определялась реканализация и более проксимальных сегментов вен, степень которой в группах различалась. В данной статье мы приводим динамику степени реканализации подвздошного сегмента, поскольку восстановление проходимости в нем происходит в самую последнюю очередь и, в целом, определяет венозную гемодинамику после перенесенного острого тромбоза [4].
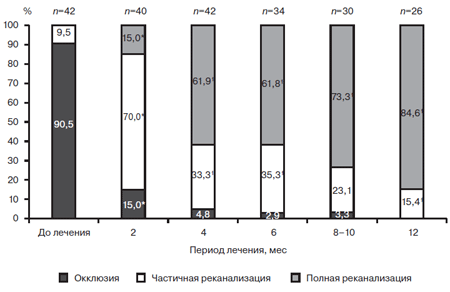
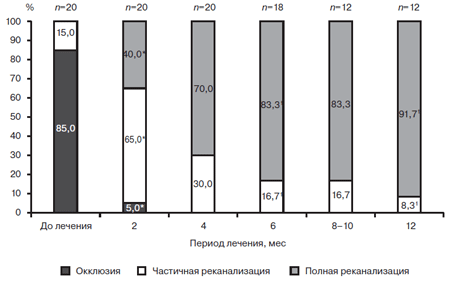
Как видно из представленных в табл. 1 данных, через 1 месяц после начала лечения ни у одного больного еще не было признаков хорошей реканализации подвздошных вен, при этом полное ее отсутствие определялось в 1 группе у 31,6% больных, во 2 группе – у 27,3%, в 3 группе – у 19,4%. Доля больных со слабой и средней степенью реканализации на этом этапе исследования в разных группах статистически значимо не различалась. Различие начинало определяться спустя 3 месяца лечения. Так, у больных 1 группы в 13,2% случаев сохранялась окклюзия проксимального сегмента, в то время как у всех пациентов 2 и 3 групп определялись в той или иной степени признаки восстановления проходимости подвздошных вен. Еще большее различие отмечалось на более поздних этапах наблюдения – через 6 и 12 месяцев лечения. Так, у больных 1 группы сохранялась окклюзия подвздошного сегмента в 13,2% случаев и через 6, и через 12 месяцев наблюдения. Хорошая же реканализация через 6 месяцев наступила у 44,7% пациентов 1 группы, у 63,6% больных 2 группы и у 80,7% пациентов 3 группы. Через 12 месяцев хорошая реканализация наблюдалась у 50% больных 1 группы, 75,8% больных 2 группы и подавляющего большинства (93,6% пациентов) 3 группы. Важно отметить, что у пациентов 2 и 3 групп через 6 и 12 месяцев наблюдения не было выявлено не только случаев окклюзии подвздошного сегмента, но и слабой реканализации: в единичных случаях наблюдалась средняя степень реканализации и в большинстве – хорошая. Обращало также на себя внимание то, что сформировавшаяся к трем месяцам наблюдения окклюзия вены у больных 1 группы в дальнейшем не претерпевала каких-либо изменений, в то время как начавшаяся реканализация постепенно прогрессировала. Было отмечено, что более ранние признаки реканализации способствовали более полному и быстрому процессу восстановления проходимости магистрального венозного русла, что наблюдалось преимущественно у пациентов 2 и 3 групп, в то время как у больных 3 группы к концу периода наблюдения в подавляющем большинстве случаев были выявлены наиболее выраженные положительные результаты лечения. В связи с этим становится очевидным, что для более полного восстановления проходимости магистральных вен нижних конечностей после перенесенного ИФФТ требуется более раннее назначение адекватной антикоагулянтной терапии, одним из вариантов которой может быть ривароксабан. Добавление же к терапии с первых суток лечения оригинального высокоочищенного диосмина способствует более быстрому и полному наступлению клинического эффекта.
Таблица 1. Степень реканализации подвздошных вен
при лечении острого илиофеморального тромбоза.
| Срок наблюдения | Степень реканализации | 1 группа (n=38) |
2 группа (n=33) |
3 группа (n=31) |
|---|---|---|---|---|
| 1 месяц | Окклюзия | 12 (31,6%) | 9 (27,3%) | 6 (19,4%) |
| Слабая | 21 (55,3%) | 18 (54,5%) | 20 (64,5%) | |
| Средняя | 5 (13,1%) | 6 (18,2%) | 5 (16,1%) | |
| Хорошая | 0 | 0 | 0 | |
| 3 месяца | Окклюзия | 5 (13,1%) | 0 | 0 |
| Слабая | 18 (47,4%) | 11 (33,3%) | 7 (22,6%) | |
| Средняя | 7 (18,4%) | 13 (39,4%) | 14 (45,2%) | |
| Хорошая | 8 (21%) | 9 (27,3%) | 10 (32,2%) | |
| 6 месяцев | Окклюзия | 5 (13,2%) | 0 | 0 |
| Слабая | 6 (15,8%) | 0 | 0 | |
| Средняя | 10 (26,3%) | 12 (36,4%) | 6 (19,4%) | |
| Хорошая | 17 (44,7%) | 21 (63,6%) | 25 (80,6%) | |
| 12 месяцев | Окклюзия | 5 (13,2%) | 0 | 0 |
| Слабая | 6 (15,8%) | 0 | 0 | |
| Средняя | 8 (21%) | 8 (24,2%) | 2 (6,5%) | |
| Хорошая | 19 (50%) | 25 (75,8%) | 29 (93,5%) |
При анализе динамики скорости кровотока в подколенной вене, несмотря на то, что первые признаки ее реканализации были выявлены у многих пациентов уже на 10 сутки лечения во всех группах, корректное определение скоростных показателей на этом этапе было невозможно. Поэтому мы проводили сравнение скорости тока крови в процессе лечения с показателем, регистрируемым через 1 месяц наблюдения, когда у всех больных отмечалась достаточная реканализация подколенной вены и можно было с большой долей достоверности определить скорость кровотока. Подколенная вена была выбрана потому, что, с одной стороны, в ней быстрее, чем в более проксимальных сегментах восстанавливается кровоток, а с другой – в отличие от вен голени кровоток в подколенной вене имеет более постоянную и достоверную величину.
Как видно из данных, представленных в табл. 2, имелись статистически значимые различия между группами на всех этапах наблюдения. Так, через 3 месяца скорость кровотока в подколенной вене в 1 группе увеличилась на 17,2±3,1%. При этом скорость кровотока у больных 2 группы была больше в 1,5 раза (p
| Срок наблюдения | 1 группа (n=38) |
2 группа (n=33) |
3 группа (n=31) |
|---|---|---|---|
| 3 месяца | 17,2±3,1 | 25,8±3,4* | 36,2±3,8* # |
| 6 месяцев | 21,4±5,3 | 49,1±3,5* | 58,7±3,2* # |
| 12 месяцев | 36,0±6,8 | 67,9±4,1* | 81,3±4,5* # |
Примечание: * – p 
Ежегодно регистрируется 60-150 случаев венозного тромбоза на 100 тысяч человек. У каждого восьмого пациента подобное состояние осложняется тромбоэмболией легочной артерии, которая в половине случаев приводит к летальному исходу. Для спасения жизни важно своевременное лечение. Важным мероприятием по предотвращению тяжелых и опасных последствий тромбоза является реканализация вен.
- Реканализация вен. Что это? Классификация.
- Диагностика сосудов
- Медикаментозная реканализация
- Тромболитическая терапия
- Использование антикоагулянтов
- Антиагрегантная и ангиопротекторная терапия
- Хирургическая реканализация
- Видео: реканализация и стентирование ПБА
- Общее описание
- Факторами риска развития тромбоза глубоких вен являются:
- УЗ-признаки пристеночного тромбоза:
- Симптомы заболевания
- Проведение диагностики
- Медикаментозная реканализация
- Необходимость оперативного вмешательства
Реканализация вен. Что это? Классификация.
Реканализация – процесс восстановления проходимости сосуда, просвет которого закрыт тромбом. Реканализация вены происходит одним из трех путей:
- естественная;
- медикаментозная;
- хирургическая.
Естественная реканализация – физиологический процесс. Она происходит под воздействием асептического фибринолиза. Сгусток устраняется самостоятельно практически в половине случаев. Помимо разрушения тромба возможна его реваскуляризация: он прорастает микрососудами, коллагеновыми структурами. Происходит восстановление проходимости сосуда и ускорение разрушения сгустка. Самостоятельное устранение закупорки возможно на этапе «рыхлого» тромба. При обрастании его соединительной таканью фибринолиз затруднен.
У здоровых людей реканализация происходит под воздействием белка плазмина спустя несколько дней после формирования закупорки – на начальной стадии развития.
Однако иногда организм не справляется с растворением тромба: сгущение крови, увеличение активности свертывания, генетическая предрасположенность, нарушение венозного кровообращения затрудняют этот процесс. Образовавшийся сгусток перекрывает просвет сосуда, может вызывать эмболию – опасное для жизни состояние. В этих случаях показана медицинская реканализация.
Диагностика сосудов

Необходимость проведения медицинской реканализации определяется с помощью инструментальных методов исследования. Состояние сосудов и степень нарушения кровотока оцениваются следующими методами:
- дуплексного сканирования – определения скорости кровотока по исследуемому сосуду и анатомические дефекты вен и артерий;
- ангиографии — рентгенологического метода, с помощью которого путем введения контраста обнаруживаются препятствия на пути кровотока: тромбы, сужения;
- компьютерной и магнитно-резонансной томографии — высокоточных методов диагностики, позволяющих обнаружить патологические процессы во всех органах и тканях, в том числе в кровеносных сосудах.
Медикаментозная реканализация
Консервативная, или медикаментозная, реканализация проводится при отсутствии угрозы жизни пациента. В ее основе лежит использование лекарственных средств, способствующих процессу восстановления сосудистого русла и разрушения тромба. Медикаментозная реканализация проводится в течение первых 3 суток с момента образования сгустка, а наибольшая эффективность достигается при проведении терапии в первые 6 часов. Применяются следующие виды препаратов:
- антикоагулянты;
- антиагреганты;
- тромболитические средства;
- ангиопротекторы.
Тромболитическая терапия
Тромболитические препараты (фибринолитики) запускают процесс рассасывания тромбов. В основе их действия лежит трансформация плазминогена в плазмин. Это белок в свою очередь расщепляет фибрин – основу тромба. Применение фибринолитиков имеет ряд противопоказаний, несоблюдение которых может спровоцировать опасные для жизни состояния, поэтому их прием должен проводиться только по назначению врача.
Применяются фибринолитики 3 групп:
- 1 поколения (Стрептокиназа, Урокиназа);
- 2 поколения (Альтеплаза, Проурокиназа, Актилаза);
- 3 поколения (Ретаплаза, Тенектеплаза).
Препараты 1 поколения – эффективные средства, однако они часто вызывают аллергию, также для них характерно действие на фибриноген и протромбин, факторы свертывания крови. Это создает опасность кровотечения. Недостатки первых лекарственных средств сглажены в препаратах 2 и 3 поколения. Они имеют избирательное действие и оказывают влияние на тромб. Эффекты разжижения крови не настолько выражены, как при использовании Стрептокиназы и Урокиназы.
Использование антикоагулянтов
Для ограничения роста закупорки сосуда применяются антикоагулянты. Использование их целесообразно именно для остановки увеличения диаметра и длины сгустка, влияние на рассасывание не так выраженно, как у тромболитиков. По механизму действия антикоагулянты классифицируются на средства прямого и непрямого действия. 
Непрямые препараты снижают синтез витамина K в печени, вследствие этого тормозится образование тромбина. К ним относятся: дикумарины, монокумарины и индандионы. Прямые антикоагулянты влияют на факторы свертывания. Среди них: гепарин, гирудин, гидроцитрат натрия, данапароид.
Выбор группы препарата зависит от тяжести состояния больного, сопутствующих заболеваний и состояния свертывания. Для оценки последнего существует анализ – коагулограмма, она отображает активность системы крови в ходе лечения антикоагулянтами.
Антиагрегантная и ангиопротекторная терапия
Антиагрегантные средства блокируют агрегацию тромбоцитов. Для этих целей применяется ацетилсалициловая кислота (аспирин). Этот один из недорогих и распространенных препаратов используется для профилактики образования новых сгустков и остановки роста существующих.
Ангиопротекторы (Пентоксифиллин, Пармидин) повышают венозный тонус и снижают проницаемость капилляров. Вследствие этого уменьшается застой крови и увеличивается ее возврат к сердцу, уменьшается отечность капилляров, повышается их устойчивость, нормализуется микроциркуляция в пораженных тканях, снижается тромбообразование и улучшаются реологические свойств крови.
Хирургическая реканализация

В случае вероятности отрыва тромба, при закупорке вены жизненно важного органа, когда ожидание эффекта от приема медикаментозных средств недопустимо, проводится реканализация вен хирургическим путем. Также операция назначается при неэффективности лекарственной терапии. В таком случае предварительно отменяются антикоагулянты, так как их прием может спровоцировать кровотечение.
Проводятся следующие типы хирургической реканализации:
- Удаление тромба проводится малоинвазивно, используются методы эндоваскулярной терапии. Под местной анестезией выполняется разрез, в поврежденный сосуд вводится катетер и под контролем оперирующего врача подводится к месту локализации тромба. Далее сгусток захватывается и извлекается из вены.
- Шунтирование используется при невозможности удаления сгустка. Формируется обходной путь кровотока. Материалом служат собственные сосуды – вены, взятые для пластики, либо синтетические аналоги.
- Перевязка предполагает наложение лигатуры выше и ниже места сгустка, кровоток перераспределяется по мелким артериям и венам.
- Стентирование – вставка баллончика, расширяющего сосуд. Улучшается кровообращение и снижается агрегация тромбоцитов на пораженной стенке, но такая операция целесообразна лишь при постепенном тромбообразовании.
Не всегда операция проводится для восстановления кровотока. Реканализация пупочной вены выполняется для обеспечения доступа к печени и желчному пузырю при их патологии. Через катетер вводятся инфузионные растворы, при гнойном поражении органов к очагу доставляются антибактериальные средства.
Тромбоз вен нижних конечностей встречается у 10-20% населения. Это заболевание проявляется недостаточностью кровообращения и трофическими нарушениями. Для более полной реканализации глубоких вен необходимо проведение комплексной терапии: прием медикаментов, соблюдение режима, использование компрессионного трикотажа, при необходимости хирургическое лечение.
Реканализация тромба – зачастую длительный процесс, требующий внимания не только врачей, но и пациентов. Для достижения лучшего результата, а также для профилактики дальнейшего тромбообразования, пациент должен пересмотреть образ жизни, соблюдать диету и своевременно обращаться к врачу при первых симптомах болезни. Достижения современной медицины позволяют значительно увеличить вероятность полного выздоровления.
Видео: реканализация и стентирование ПБА
Общее описание
Посттромботическая болезнь нижних конечностей (ПТБ) — это заболевание, формирующееся после перенесенного тромбоза глубокой венозной системы с частичным или полным разрушением клапанного аппарата, приводящее к постоянному венозному застою и развитию трофических расстройств.
Таким образом ПТБ является следствием перенесенного флеботромбоза. При рассасывании тромба в просвете сосуда со сгустком частично разрушается и клапанный аппарат, что неизбежно приводит к венозному застою и прогрессированию процесса.
Факторами риска развития тромбоза глубоких вен являются:
- возраст старше 60 лет;
- тяжелая операция или травма;
- злокачественные новообразования;
- беременность и применение оральных контрацептивов.
По данным зарубежной литературы, наибольшим риском сопровождаются ортопедические и абдоминальные операции, а также вмешательства под общим обезболиванием, сопровождающиеся иммобилизацией. Другими причинами венозного тромбоза являются врожденные или приобретенные тромбофилии.
УЗ-признаки пристеночного тромбоза:
- при компрессии датчиком вена не сжимается.
- в В-режиме просвет вены заполнен тромботическими массами различной эхогенности;
- диаметр тромбированной вены увеличен по сравнению со здоровой контрлатеральной стороной (на ранних стадиях заболевания);
- отсутствуют изменения диаметра вены при дыхании;
- кровоток в допплеровских режимах не лоцируется;
- в некоторых случаях наблюдается компенсаторное расширение притоков поверхностных или глубоких вен.
- при компрессии датчиком вена сжимается не полностью;
- тромб визуализируется как расположенная в просвете вены структура различной эхогенности, при этом между тромбом и стенками вены наблюдается свободное пространство (то есть отсутствует фиксация проксимальной части тромба к стенкам вены);
- в режиме ЦДК в проксимальном сегменте между стенками вены и тромбом определяется кровоток (циркулярное окрашивание);
- верхушка тромба совершает свободные колебательные движения в просвете вены, движется асинхронно со стенкой.
- при компрессии датчиком вена сжимается не полностью;
- тромботические эхомассы неподвижны вследствие того, что спаяны с одной из стенок вены; в режиме ЦДК на участке тромба просвет вены окрашивается не полностью;
- в спектральном режиме определяется монофазный кровоток или кровоток, синхронизированный с дыханием.
Сегментарный тромбоз клинически часто протекает бессимптомно.
Обычно местом первичного тромбообразования является створка венозного клапана или клапанный синус. Тромбозы часто локализуются первично в синусах венозных клапанов и распространяются по ходу вены.
Тромбоз — не статичное состояние, а динамичный процесс.
Симптомы заболевания

Выделяют ряд типичных симптомов, характерных для данного заболевания. Основным по значимости признаком является отечность пораженной конечности (отечность носит постоянный характер и усиливается после физической нагрузки).
Постепенно изменяется окраска кожного покрова (чаще всего в месте предполагаемого перфоранта). Кожный покров грубеет, уплотняется и формируется так называемая индурация.
В конечном итоге развиваются трофические расстройства в виде язвенных дефектов, которые длительное время не заживают.
Проведение диагностики
Состояние сосудов и степень реканализации показывает дуплексное сканирование, которое совмещает достоинства ультразвукового исследования и допплерографии. Это неинвазивный метод, помогающий определить скорость кровотока и анатомические недостатки артерий и вен (наличие бляшек, петрификатов, тромбов, реканализации сосудов).
Для оценки реологических свойств крови пациент сдает коагулограмму, которая оценивает основные показатели гемостаза: протромбин, фибриноген, протромбиновое и тромбиновое время. Под контролем этих показателей ведется терапия прямыми и непрямыми антикоагулянтами.
Реканализация тромба предусмотрена природой, но иногда для этого может потребоваться врачебная помощь с медикаментозными и хирургическими методами.
- Консультация сосудистого хирурга и осмотр.
- Дуплексное сканирование сосудов (с помощью этого метода легко определить проходимость вен, оценить работу клапанного аппарата и решить вопрос о дальнейшей тактике лечения).
Диагностика основывается на характерных клинических проявлениях заболевания, а также на имеющемся в анамнезе факте перенесенного тромбоза вен нижних конечностей (3 месяца назад и ранее). В большинстве случаев опытный хирург или флеболог уже при внешнем осмотре может установить диагноз, обозначить стадию и форму посттромботической болезни, локализацию патологических изменений.
Для назначения лечения и более детального изучения венозно-клапанной системы нижних конечностей могут быть проведены следующие методы диагностики:
- флебография;
- кавография;
- дуплексное ангиосканирование вен;
- МРТ-ангиосканирование вен;
- КТ вен нижних конечностей с контрастированием;
- внутрисосудистое ультразвуковое исследование вены.
Дифференциальный диагноз в обязательном порядке проводится с патологиями, имеющими схожее течение и симптоматику. Это — тяжелая стадия варикоза, лимфедема, отеки ног на фоне тяжелой сердечной, почечной недостаточности. У больного могут проявиться врожденные артериовенозные свищи, что также следует учитывать при дифдиагностике.
Медикаментозная реканализация
Тромбообразование — естественный процесс при повреждении сосуда для предотвращения кровотечения, опасного для жизни. Однако сам тромб может нести смертельную угрозу в случае его отрыва и эмболизации крупного сосуда (сердца, легочного ствола, мозга). В здоровом организме система гемостаза (кровесвертывающие факторы) уравновешивается системой фибринолиза.
Тромб залатывает поврежденный сосуд, восстанавливается соединительная ткань. Затем действует система фибринолиза. Под воздействием фибринолитической системы тромб лизируется (растворяется), восстанавливается проходимость.
Иногда тромб организуется, т. е. обрастает соединительной тканью, в которой появляются полости мелкого диаметра, становящиеся в дальнейшем сосудами. Этот процесс называется канализацией тромба.
Когда происходит тромбоз коронарных артерий, главных артерий мозга, или легочной артерии, пациенту необходима врачебная помощь, т.к. возможна смерть. Миокард и мозг — наиболее чувствительные к недостатку кровообращения органы.
Мозг выдерживает гипоксию в течение лишь 5-7 минут. Опасна также тромбоэмболия легочной артерии, бедренной артерии, чревного ствола, брыжеечных артерий.
Обструкция тромбом может приводить к гангренозным процессам в органе.
В таких случаях врачи применяют фибринолитические препараты и антикоагулянты для реканализации. Фибринолитики (Стрептокиназа, Алтеплаза, Урокиназа) вводят внутривенно. Прямые антикоагулянты вводят как внутривенно, так и подкожно.
Для расширения артерий мозга и налаживания кровообращения назначаются Циннаризин, Кавинтон и т. д.
При ишемической болезни сердца для расширения коронарных артерий применяют органические нитраты и донаторы окиси азота (Нитроглицерин, Нитропруссид натрия), блокаторы кальциевых каналов (Нифедипин, Амлопидин, Верапамил).
При тромбозе вен для ускорения их реканализации применяют:
- Ангиопротекторы.
- Антиагреганты.
- Антикоагулянты.
Для реканализации артерий и вен иногда применяют хирургическое вмешательство. Тромб удаляется из сосуда. Если удаление тромба невозможно, то выполняют наложение шунта — обходного кровеносного пути. Материалом для шунта служат собственные вены, взятые для пластики, либо синтетические материалы.
" alt="">
Также в сосудистой хирургии применяется стентирование. Стент применяется для восстановления проходимости сосуда и расширения его просвета.
Если нет опасного для жизни состояния (риск отрыва тромба или уже произошедшая закупорка жизненно важных сосудов), то сначала применяется консервативное лечение. В зависимости от места тромбообразования подбирается медикаментозное средство.
Необходимость оперативного вмешательства
Как уже говорилось выше, хирургическое лечение проводится только в том случае, если медикаментозное тормборазрушение несет опасность жизни или здоровью пациента.
Для лечения может использоваться:
- Шунтирование. Участок с тромбом удаляется и производится замена затромбированного участка сосудом, взятым из другой части тела, или синтетическим протезом.
- Перевязка. Накладываются лигатуры выше и ниже образовавшегося сгустка, при этом кровоток перераспределяется по более мелким артериям или венам.
- Удаление сгустка. Большая часть тромба удаляется хирургическим путем, а для более полного очищения сосудистой стенки дополнительно используются ангиопротекторы и антикоагулянты.
- Стентирование. Применяется тогда, когда тромбообразование происходит постепенно, вызывая сужение сосудистого русла. Вставка стента (баллончика, расширяющего вены или артерии) способствует улучшению кровотока и препятствует дальнейшей агрегации тромбоцитов на сосудистой стенке.
Кроме оперативного восстановления проходимости сосудов, при риске отрыва тромбов широко применяется для профилактики отрыва тромба установка кава-фильтра.
Небольшая конструкция, похожая на сетчатый зонтик, устанавливается в сосуде выше места тромбообразования, она не препятствует кровообращению, но способна задержать оторвавшийся кровяной сгусток и предотвратить возможные осложнения. Дальнейшее лечение после установки фильтра проводится кроворазжижающими и сосудорасширяющими препаратами.







